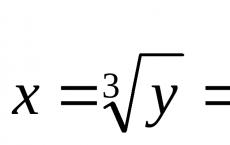Kimyasal maddeler. Madde nedir? Maddelerin sınıfları nelerdir
anlamında madde kavramına yakındır, ancak tam olarak eşdeğer değildir. "Madde" kelimesi esas olarak, yalnızca mekanik yasaların hakim olduğu kaba, hareketsiz, ölü gerçeklik hakkındaki fikirlerle ilişkilendirilirken, madde, bir formun alınması nedeniyle form, yaşam hakkında düşünceleri uyandıran bir "madde" dir. uygunluk, soyluluk. Gestalt dokumaya bakın.
Mükemmel Tanım
Eksik tanım ↓
Madde
maddenin türüne göre. Dinlenme kütlesine sahip bir dizi ayrık oluşum.
"Görünüm" tanımı morfolojiktir, doğrudur, ancak bizi tatmin edemez, çünkü bu tamamen sınıflandırıcı bir bölümdür ve gerçekte ilk yaklaşımda hiçbir şeyin karşılık gelmediği bir bölümdür.
Maddenin "saf haliyle" boşluk (ilk nesne) olduğuna dair bir hipotez vardır. O halde: Madde, maddi dünyanın nesnelerinden biridir (beşinci nesne); Duran dalga formundaki madde, temel bir parçacık (elektron, pozitron, proton, nötron vb.) oluşturur - ilerleyen dalga formundaki dördüncü nesne - bir foton (üçüncü nesne) ve bunların kombinasyon atomu - madde. İkinci nesne alandır (bir yayın mekanik gerilimine benzer şekilde vakum gerilimi).
Burada hayal kurabilirsiniz: bir boşluk (ilk nesne) ve başka bir şey (sıfır nesne), örneğin apeiron, Evrensel Zihin, Tanrı vb., yani Dünyamızın algısının dışında olan bir şey ve boşlukla etkileşimi alan ve maddeyi verir, daha da gelişmesi (hareket ve dönüşümü) Yaşam dahil Dünyanın tüm çeşitliliğini yaratır. Bu fantezi, madde kavramına dayanan Dünya hakkındaki görüş sistemiyle "gözlemimize açık" bir şey olarak çelişiyor.
Başka bir seçenek: madde, alan ve vakum, maddenin farklı halleridir (suyun farklı hallerde olabilmesine benzer: gaz, sıvı, katı).
Vakum bozulmamış bir durumdur, alan stresli bir durumdur, madde ise salınımlı bir durumdur. Fikri daha da geliştirerek şunu elde ederiz: hareketsiz madde - boşluk, içinde hareket eden bir voltaj dalgası - bir alan, bir foton, hareketli bir duran dalga paketi - bir madde.
Eksik tanım ↓
Madde kavramı aynı anda birkaç bilim tarafından incelenmektedir. Hangi maddelerin olduğu sorusunu iki açıdan analiz edeceğiz - kimya bilimi açısından ve fizik açısından.
Kimya ve fizikte madde
Kimyacılar maddeyi belirli bir dizi kimyasal element içeren fiziksel bir madde olarak anlarlar. Modern fizikte madde, fermiyonlardan oluşan bir madde veya fermiyonlar, bozonlar içeren, durgun kütlesi olan bir tür madde olarak kabul edilir. Her zamanki gibi madde parçacıklardan, çoğunlukla da elektronlardan, protonlardan ve nötronlardan oluşmalıdır. Protonlar ve nötronlar atom çekirdeğini oluşturur ve bu elementler birlikte atomları (atomik madde) oluşturur.
Madde özellikleri
Hemen hemen her maddenin kendine has özellikleri vardır. Özellikler, bir maddenin bireyselliğini gösteren ve dolayısıyla diğer tüm maddelerden farklılıklarını gösteren özellikler olarak anlaşılmaktadır. Karakteristik fizikokimyasal özellikler sabitlerdir - yoğunluk, Çeşitli türler sıcaklıklar, termodinamik, kristal yapı göstergeleri.
Maddelerin kimyasal sınıflandırması
Kimyada maddeler bileşiklere ve bunların karışımlarına ayrılır. Ayrıca organik maddeler de söylenmelidir: Bileşik, belirli kalıpları dikkate alarak birbirine bağlanan bir dizi atomdur. Bir bileşik ile bir madde karışımı arasındaki sınırın açıkça tanımlanmasının oldukça zor olduğu unutulmamalıdır. Bunun nedeni bilimin değişken bileşime sahip maddeleri bilmesidir. Onlar için kesin bir formül yapmak mümkün değil. Ek olarak bileşik genel olarak bir soyutlamadır, çünkü pratik anlamda incelenen maddenin yalnızca nihai saflığına ulaşılabilir. Mevcut olan herhangi gerçek hayat bir numune, maddelerin bir karışımıdır, ancak tüm gruptan bir maddenin baskın olduğu bir durumdur. Ayrıca organik maddelerin neler olduğunu da söylemek gerekir. Bu karmaşık madde grubu karbon (proteinler, karbonhidratlar) içerir.
Basit ve karmaşık maddeler
Basit maddeler (O2, O3, H2, Cl2), yalnızca bir kimyasal elementin atomlarından oluşan maddelerdir. Bu maddeler elementlerin serbest formdaki varlığının bir şeklidir. Başka bir deyişle bunlar kimyasal elementler Diğer elementlerle bağlantısı olmayan basit maddeler oluşturur. Bu tür maddelerin 400'den fazla çeşidi bilim tarafından bilinmektedir. Basit maddeler atomlar arasındaki bağın türüne göre sınıflandırılır. Yani basit maddeler metallere (Na, Mg, Al, Bi, vb.) ve metal olmayanlara (H2, N2, Br2, Si, vb.) ayrılır.
Bileşikler iki veya daha fazla elementin birbirine bağlanmasıyla oluşan kimyasal bileşiklerdir. Basit maddeler, molekülleri kovalent bir bağla (azot, oksijen, brom, flor) birbirine bağlanan atomlardan oluşuyorsa, kimyasal bileşikler olarak adlandırılma hakkına da sahiptir. Ancak inert (soylu) gazlara ve atomik hidrojene kimyasal bileşikler demek yanlış olur.
Maddelerin fiziksel sınıflandırması
Fizik açısından maddeler çeşitli toplanma durumlarında bulunur: vücut, sıvı ve gaz. Örneğin çıplak gözle hangi katıların görülebileceği hakkında. Aynı şey diğer toplanma durumu için de söylenebilir. Doğada hangi sıvı maddelerin bulunduğunu okuldan biliyoruz. Su gibi bir maddenin buz, sıvı su ve buhar gibi aynı anda üç durumda bulunabilmesi dikkat çekicidir. Bir maddenin üç toplam durumu, maddelerin bireysel özellikleri olarak kabul edilmez, ancak maddelerin varlığına ilişkin dış koşullara bağlı olarak farklı olanlara karşılık gelir. Toplu devlet durumlarından gerçek devletlere geçişte kimyasal Bilimde amorf veya camsı hallerin yanı sıra sıvı kristal hali ve polimer hali olarak adlandırılan bir dizi ara tip tanımlanabilir. Bu bağlamda bilim adamları sıklıkla "faz" kavramını kullanırlar.
Fizik, diğerlerinin yanı sıra, kimyasal bir maddenin dördüncü toplanma durumunu da dikkate alır. Bu bir plazmadır yani tamamen veya kısmen iyonize olmuş bir durumdur ve bu haldeki pozitif ve negatif yüklerin yoğunluğu aynıdır yani plazma elektriksel olarak nötrdür. Genel olarak doğada pek çok madde var ama artık maddelerin ne olduğunu biliyorsunuz ve bu çok daha önemli.
Hayatta çeşitli bedenler ve nesnelerle çevriliyiz. Örneğin, iç mekanda bir pencere, bir kapı, bir masa, bir ampul, bir bardak, sokakta ise bir araba, trafik ışığı, asfalt var. Herhangi bir cisim veya nesne maddeden oluşur. Bu makale bir maddenin ne olduğunu tartışacak.
Kimya nedir?
Su önemli bir çözücü ve stabilizatördür. Güçlü ısı kapasitesine ve termal iletkenliğe sahiptir. Su ortamı temel kimyasal reaksiyonların oluşmasına elverişlidir. Şeffaftır ve pratik olarak sıkıştırmaya karşı dayanıklıdır.
İnorganik ve organik maddeler arasındaki fark nedir?
Bu iki madde grubu arasında özellikle güçlü dış farklılıklar yoktur. Temel fark, inorganik maddelerin moleküler olmayan bir yapıya sahip olduğu ve organik maddelerin moleküler bir yapıya sahip olduğu yapıda yatmaktadır.
İnorganik maddeler moleküler olmayan bir yapıya sahiptir, bu nedenle aşağıdakilerle karakterize edilirler: yüksek sıcaklıklar erime ve kaynama. Karbon içermezler. Bunlara soy gazlar (neon, argon), metaller (kalsiyum, kalsiyum, sodyum), amfoterik maddeler (demir, alüminyum) ve metal olmayanlar (silikon), hidroksitler, ikili bileşikler, tuzlar dahildir.
Moleküler yapıya sahip organik maddeler. Yeterince var Düşük sıcaklık erir ve ısıtıldığında hızla ayrışırlar. Çoğunlukla karbondan oluşur. İstisnalar: karbürler, karbonatlar, karbon oksitleri ve siyanürler. Karbon, çok sayıda karmaşık bileşiğin oluşumuna izin verir (doğada 10 milyondan fazlası bilinmektedir).
Sınıflarının çoğu biyolojik kökene aittir (karbonhidratlar, proteinler, lipitler, nükleik asitler). Bu bileşikler arasında nitrojen, hidrojen, oksijen, fosfor ve kükürt bulunur.

Bir maddenin ne olduğunu anlamak için onun hayatımızda nasıl bir rol oynadığını hayal etmek gerekir. Diğer maddelerle etkileşime girerek yenilerini oluşturur. Onlar olmadan, çevredeki dünyanın hayati faaliyeti ayrılamaz ve düşünülemez. Tüm nesneler belirli maddelerden oluştuğundan hayatımızda önemli bir rol oynarlar.
Bağıl moleküler kütle - kütle (amu) 6,02 × 10 Kompleks bir maddenin 23 molekülü. Sayısal olarak molar kütleye eşittir, ancak boyut olarak farklıdır.
- Moleküllerdeki atomlar belirli bir sırayla birbirine bağlanır. Bu diziyi değiştirmek, yeni özelliklere sahip yeni bir maddenin oluşmasına yol açar.
- Atomların bağlantısı değerliklerine göre gerçekleşir.
- Maddelerin özellikleri yalnızca bileşimlerine değil aynı zamanda " kimyasal yapı”, yani atomların moleküllerdeki bağlantı düzeninden ve karşılıklı etkilerinin doğasından. Birbirine doğrudan bağlanan atomlar birbirleri üzerinde en güçlü etkiye sahiptir.
Reaksiyonun termal etkisi içindeki akış sırasında sistem tarafından salınan veya emilen ısıdır Kimyasal reaksiyon. Reaksiyonun ısının salınmasıyla mı yoksa ısının emilmesiyle mi gerçekleştiğine bağlı olarak ekzotermik ve endotermik reaksiyonlar ayırt edilir. Birincisi, kural olarak, bağlantının tüm reaksiyonlarını ve ikinci ayrışma reaksiyonlarını içerir.
Kimyasal reaksiyonun hızı- Bir birim reaksiyon alanında birim zaman başına reaksiyona giren maddelerden birinin miktarındaki değişiklik.
Sistemin iç enerjisi- toplam enerji dahili sistem Bir bütün olarak sistemin kinetik ve potansiyel enerjisi hariç, moleküllerin, atomların, çekirdeklerin, atomlardaki elektronların, intranükleer ve diğer enerji türlerinin etkileşimi ve hareketi enerjisini içerir.
Karmaşık bir maddenin standart oluşum entalpisi (ısısı)- bu maddenin 1 molünün oluşumunun reaksiyonunun termal etkisi basit maddeler standart koşullar altında (= 298 K ve 101 kPa basınç) kararlı bir toplanma durumundadırlar.
MADDE
MADDE
fiziksel olanın aksine bir tür madde. alanlar, dinlenme kütlesine sahiptir. Sonuçta dalga, geri kalanı sıfıra eşit olmayan temel parçacıklardan oluşur. (çoğunlukla elektronlardan, protonlardan, nötronlardan). Klasik olarak V. fizik ve fiziksel. alanlar, birincisi ayrık ve ikincisi sürekli olan iki tür madde olarak birbirine kesinlikle karşıttı. İkili fikrini ortaya atan kuantum. Herhangi bir mikro nesnenin parçacık dalga doğası, bu karşıtlığın düzleşmesine yol açtı. Su ile alan arasındaki yakın ilişkinin açığa çıkması, maddenin yapısı hakkındaki fikirlerin derinleşmesine yol açtı. Bu temelde, V. ve madde baştan sona kesin olarak sınırlandırılmıştı. pl. Yüzyıllar boyunca hem felsefe hem de bilimle özdeşleşmiş ve Felsefeönem madde kategorisinde kaldı ve V. fizik ve kimyadaki bilimsel olanı korudu. Vakum karasal koşullar altında dört durumda meydana gelir: gazlar, sıvılar, katılar ve plazma. V.'nin özel, süper yoğun bir formda da bulunabileceği belirtiliyor. (örneğin nötronda) durum.
Vavilov S. I., Madde fikrinin gelişimi, Sobr. operasyon, T. 3, M., 1956, İle.-41-62; Maddenin yapısı ve biçimleri. [Doygunluk. Art.], M., 1967.
I. S. Alekseev.
Felsefi ansiklopedik sözlük. - M .: Sovyet Ansiklopedisi. Ch. editörler: L. F. Ilyichev, P. N. Fedoseev, S. M. Kovalev, V. G. Panov. 1983 .
MADDE
anlam olarak kavrama yakın konu, ama tamamen eşdeğer değil. "" kelimesi esas olarak, yalnızca mekanik yasaların hakim olduğu kaba, hareketsiz, ölü gerçeklik hakkındaki fikirlerle ilişkilendirilirken, madde, bir formun alınmasından dolayı formu, hayata uygunluğu, asaleti çağrıştıran bir "materyaldir". . Santimetre. Gestalt dokuma.
Felsefi Ansiklopedik Sözlük. 2010 .
MADDE
maddenin temel formlarından biridir. V. makroskobik içerir. tüm toplanma durumlarındaki cisimler (gazlar, sıvılar, kristaller, vb.) ve bunları oluşturan ve kendi kütlelerine ("dinlenme kütlesi") sahip parçacıklar. V.'de çok sayıda parçacık türü bilinmektedir: "temel" parçacıklar (elektronlar, protonlar, nötronlar, mezonlar, pozitronlar vb.), atom çekirdekleri, atomlar, moleküller, iyonlar, serbest radikaller, kolloidal parçacıklar, makromoleküller vb. (bkz. Maddenin temel parçacıkları).
Aydınlatılmış.: Engels F., Doğanın Diyalektiği, Moskova, 1955; kendi, Anti-Dühring, M., 1957; V. I. Lenin, Materyalizm ve ampiryo-kritisizm, Soch., 4. baskı, cilt 14; Vavilov S. I., Madde fikrinin gelişimi, Sobr. soch., cilt 3, M., 1956; onun, Lenin'in ve modern, aynı eserde; kendi eseri, Lenin ve modern fiziğin felsefi sorunları, aynı eser; Goldansky V., Leikin E., Atom çekirdeğinin dönüşümleri, M., 1958; Kondratiev V.N., Yapı ve Kimyasal özellikler moleküller, M., 1953; "Fiziksel Bilimlerdeki Gelişmeler", 1952, cilt 48, no. 2 (kütle ve enerji sorununa adanmıştır); Ovchinnikov N. F., Kütle ve enerji kavramları ..., M., 1957; Kedrov B. M., Kimyada element kavramının evrimi, M., 1956; Novozhilov Yu.V., Temel parçacıklar, Moskova, 1959.
Felsefi Ansiklopedi. 5 ciltte - M.: Sovyet Ansiklopedisi. Düzenleyen: F. V. Konstantinov. 1960-1970 .
Eş anlamlı: